- No.277Shuangshan道Deqing、中国浙江省
- [email protected]
- WhatsApp+8613065722186
ジップステッチロングメッド創傷閉鎖デバイスのランダム化研究
先天性心臓手術後に使用する新しい非侵襲性ジップステッチ皮膚閉鎖装置のランダム化研究
田中 有紀 医学博士、宮本 崇史 医学博士、内藤 祐司 医学博士、
吉武修一医師、笹原章弘医師、宮地かがみ医師、博士
ぐんまこども医療センター心臓血管外科(渋川市)心臓血管外科、
北里大学病院、相模原市
バックグラウンド:
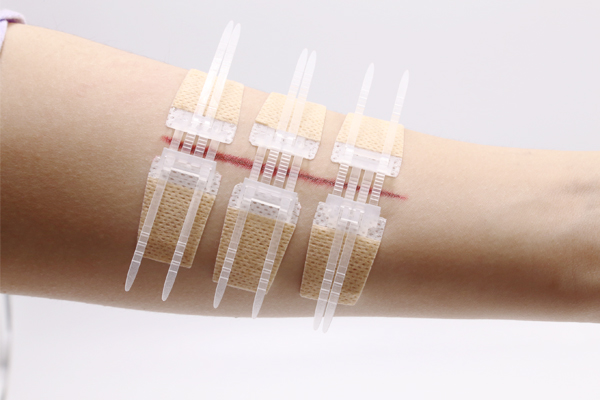
新しい非侵襲性ジップ ステッチ ロングメッドを報告します。 創傷閉鎖装置 (ZheJiang Longmed Medical Technology Co.,Ltd)。このデバイスは、手術後の美容上の結果が良好であり、手術時間を短縮すると考えられています。この研究では、Closureデバイスを使用した皮膚閉鎖と皮下縫合糸を比較し、この新しいデバイスの有用性と安全性を評価しました。
方法:
これは、2014 年 6 月から 2015 年 12 月までに胸骨正中切開による心臓手術を受けた 214 人の患者を対象とした前向き無作為化研究でした。患者 136 人中、これは初回手術群であり、そのうち 71 人の患者が創傷閉鎖装置 (閉鎖群) を受け、65 人の患者が創傷閉鎖装置を受けました。患者は皮下縫合術を受けた(縫合群)。 78 人の患者のうち、これは再手術グループであり、そのうち 42 人の患者は閉鎖グループ、36 人の患者は縫合グループでした。バンクーバー傷跡スケールを使用した美容結果は、最初の手術グループと再手術グループで別々に評価されました。
結果:
最初の手術群 (p < 0.001) と再手術群 (p [ 0.007) の間では、バンクーバー瘢痕スケール スコアの合計に有意差がありました。皮膚の閉鎖時間は、縫合グループよりも閉鎖グループの方が有意に短かった(113.0 ± 9.1 秒 vs 375.9 ± 60.2 秒、p < 0.001)。手術部位の感染率に関しては、各グループ間に有意差は見られませんでした。この装置に特有の合併症には皮膚の変色が含まれます(0.9%)、表皮剥離 (0.9%)、およびデバイスの剥離 (1.8%)。しかし、重篤な合併症は発生しませんでした。
結論:
胸骨正中切開による先天性心臓手術では、創傷閉鎖デバイスは 美容上の外観を改善し、創傷閉鎖時間を短縮するための優れた選択肢です。また、安全に使用できる装置であることが証明されました。
(Ann Thorac Surg 2016;102:1368–74) 2016 年、胸部外科医協会
手術部位の感染症と肥厚性瘢痕は主な術後創傷合併症であり、これらは心臓血管手術後に発生することがあります[1-3]。シアノアクリレート接着剤や外科用ステープルなど、いくつかの皮膚閉鎖装置の使用が報告されており [4-6]、これらの装置は皮膚閉鎖時間の短縮、外観の改善、感染率の低下に優れた可能性があることが実証されています。 。創傷閉鎖デバイス (ZheJiang Longmed Medical Technology Co.,Ltd.) は、創傷閉鎖デバイスの可能性を減らす、新しい非侵襲性の最終層皮膚閉鎖デバイスです。 創傷合併症の場合[7、8]。
ジップステッチ Longmed 創傷閉鎖デバイスの開発コンセプトは、皮膚閉鎖時間を短縮し、手術後の肥厚性瘢痕を防ぐことでした。閉鎖装置の使用は心臓血管外科以外の分野でも報告されているが、胸骨正中切開が行われた先天性患者の手術創を閉鎖するために創閉鎖装置が使用されたという報告はない。この研究では、創傷閉鎖デバイスが有用かつ安全に閉鎖できるデバイスであるかどうかを評価しました。 外科的切開 胸骨正中切開による心臓血管手術後の先天性患者。
2016 年 3 月 23 日に出版が受理されました。
宛先は、〒377-8577 群馬県渋川市北津町下箱田779番地、群馬県立こども医療センター小児心臓外科の田中医師宛。メール:[email protected]
2016 年胸部外科医協会 0003-4975/$36.00 エルゼビア発行
患者と方法
この創傷閉鎖装置の研究の研究プロトコールは、ヘルシンキ宣言に従って当院の研究審査委員会によって承認されました。
患者と研究デザイン
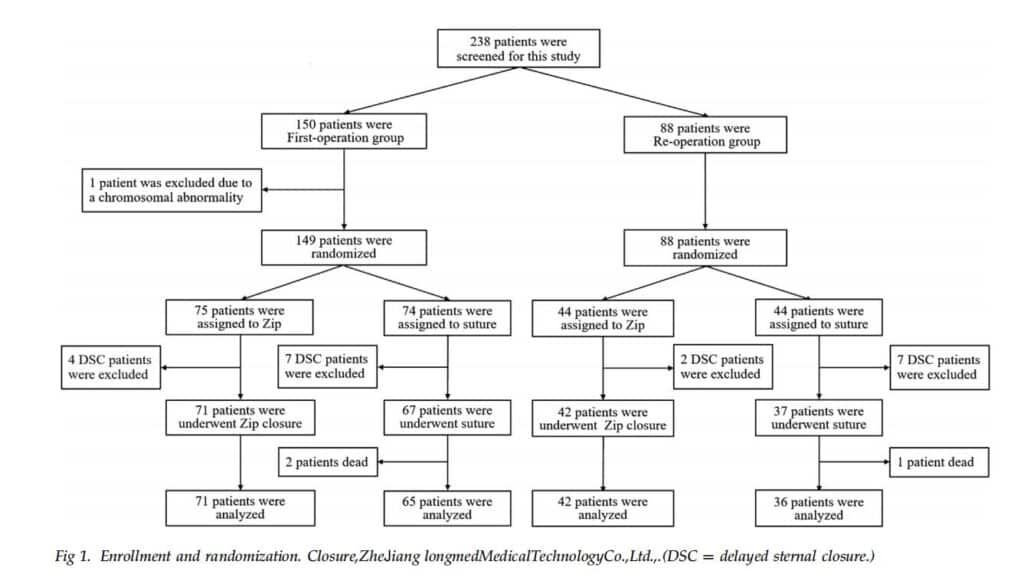
創傷閉鎖装置の研究には、2014年6月から2015年10月まで、日本の渋川市にあるぐんまこども医療センター心臓血管外科で胸骨正中切開による心臓手術を連続して受けた患者238人が対象となった。登録された患者は、計算された単純なランダム化を使用して、創傷閉鎖デバイス グループ (閉鎖グループ) または皮下縫合糸グループ (縫合グループ) にランダムに割り当てられ、研究されました。 将来的には(図1)。すべての患者は、参加するために書面によるインフォームドコンセントを提出しました。
この試験での評価を簡素化するために、胸骨閉鎖が遅れた患者および21トリソミー以外の染色体異常を有する患者は研究から除外された。この研究では、胸骨閉鎖が遅れた20人の患者、21トリソミー以外の染色体異常を患った1人の患者、および手術後3か月以内に死亡した3人の患者が除外され、214人の患者がこの研究に残った。再手術患者と21トリソミーの患者が含まれていました。
性別、年齢、体重、患者がダウン症候群であるか、乳児か新生児であるか、手術創の長さ、総手術時間、出血量などの人口統計データと臨床的特徴が収集されました。この研究で分析された結果には、美容上の外観、皮膚の閉鎖時間、合併症の発生率が含まれます。
214 人の患者を初回手術 (FO) グループまたは再手術 (RO) グループに分け、各グループの美容上の外観を分析しました。ただし、皮膚閉鎖時間と合併症率を閉鎖群と縫合群で比較するために、すべての患者をプールしました。皮膚の変色、表皮溶解、創傷閉鎖デバイスに対するアレルギー反応、創傷閉鎖デバイス特有の潜在的な合併症を事前に分析しました。
デバイスの損傷や剥離。これらの合併症は、企業から提供された情報と個人の経験に基づいて分析され、機器の損傷も含めて機器の安全性を評価しました。
装置と技術
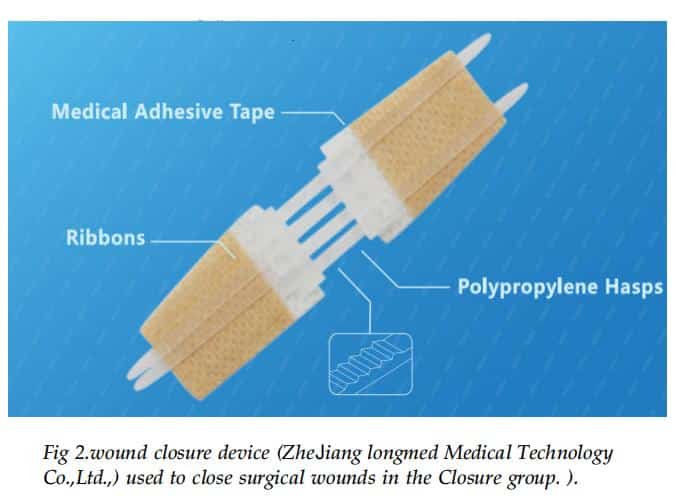
この研究に含まれた214人の患者は、心肺バイパスの有無にかかわらず、胸骨正中切開による心臓血管手術を受けました。閉鎖グループと縫合グループの両方で、皮下組織 4−0 Vicryl(オハイオ州シンシナティのエチコン)吸収性マルチフィラメント縫合糸を使用して縫合した。閉鎖グループでは、手術創の最表面を創傷閉鎖デバイスで閉鎖しました (図 2)。縫合糸群では、従来通り、縫合糸の端に外科用クリップを備えた5-0 Prolene縫合糸(Ethicon)を使用して連続皮下縫合糸を配置した。
創傷保護は、汗や浸出液で汚れた場合には消毒剤を使用せずに、滅菌ガーゼを使用して新しいガーゼに交換することで達成されました。すべての患者において、デバイスの取り外しまたは抜糸は手術の 7 日後に行われました。創傷閉鎖装置の除去は、皮膚を保護するために癒着除去剤(ニチバン、東京、文京)を使用して行われた。装置または縫合糸を除去した後、患者は入浴を許可されました。
フォローアップとデータ収集
臨床データを記録するツールとして、電子医療記録と日本の先天性心臓血管外科データベースが使用されました。すべての人口統計データと臨床的特徴データは術前に記録され、 術中。皮膚閉鎖時間を術中にストップウォッチで記録した。傷の管理 プロトコルはすべての患者に適用されました。追跡調査および合併症のデータは、術後 1、2、4、8、12 週間目に 3 人の心臓血管外科医によって収集されました。美容的外観を術後3ヶ月で記録した。退院後は、患者は当院で外来患者として経過観察された。
創傷の評価
美容上の成果の評価は、使用された皮膚閉鎖の種類を知らされていない手術後 3 か月後に 2 人の形成外科医によって行われました。美容上の外観はバンクーバー瘢痕スケール (VSS) を使用して評価されました。これは、1990 年にサリバンによって初めて記載された、広く知られている熱傷瘢痕評価スケールです。 VSS は、外科的瘢痕に対して最も頻繁に使用される評価スケールであり [9-11]、4 つの評価スケールがあります。血管分布、色素沈着、柔軟性、および身長に基づいたカテゴリ [12]。合計スコアは 0 ~ 13 の範囲で、スコア 0 は正常な皮膚を表します (表 1)。

統計的手法
StatView 5.0 ソフトウェア (SAS Institute Inc、ノースカロライナ州ケーリー) および Excel 2013 (Microsoft Corp、ワシントン州レドモンド) が使用されました。 データ分析。結果は、量的変数の期間における平均 SD または中央値および四分位範囲 (95% 信頼度) として表示され、カテゴリ変数は絶対頻度と年齢パーセントによって要約されます。連続変数は、スチューデント テストとマン-ホイットニー U テストを使用して比較されました。カテゴリ変数は、予測頻度が 5 未満の場合、Pearson X² 検定または Fisher の直接確率検定を使用して比較されました。0.05 以下の P 値は、統計的に有意であるとみなされます。
結果
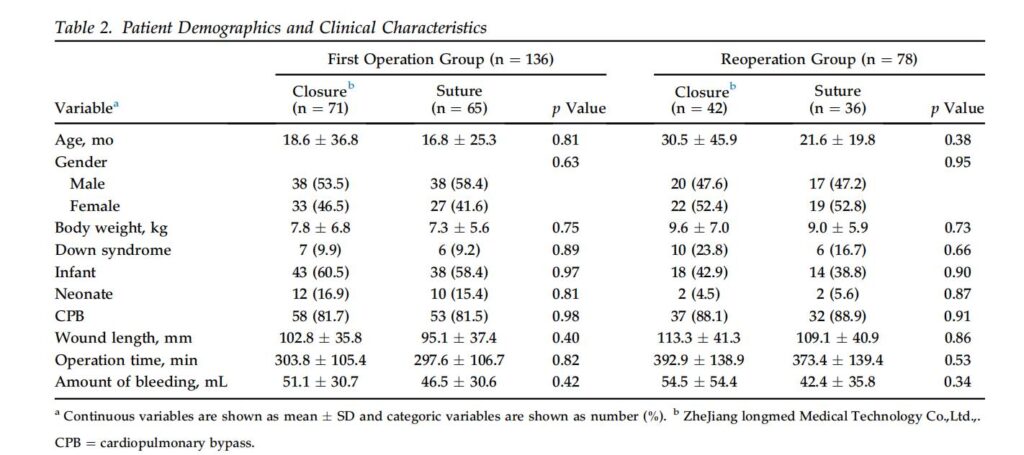
FO 群の患者数は 136 名(閉鎖群:71 名、縫合群:65 名)、RO 群の患者数は 78 名(閉鎖群:42 名、縫合群:36 名)でした。当外来では全患者を 3 年以上モニタリングしました。心臓手術から数カ月後。人口統計データと臨床的特徴を分析したところ、 グループと縫合糸グループ間の有意差 (表 2)。こちらも大きな差はありませんでした 術前の RO グループの平均 VSS スコアの合計 (閉鎖: VSS 3.2 ± 1.2; 縫合: VSS 3.3 ± 1.3; p = 0.57)。平均年齢と体重はFO群と比較してRO群の方が高く、平均総手術時間はRO群の方が長かったが、これらの結果は有意ではなかった。
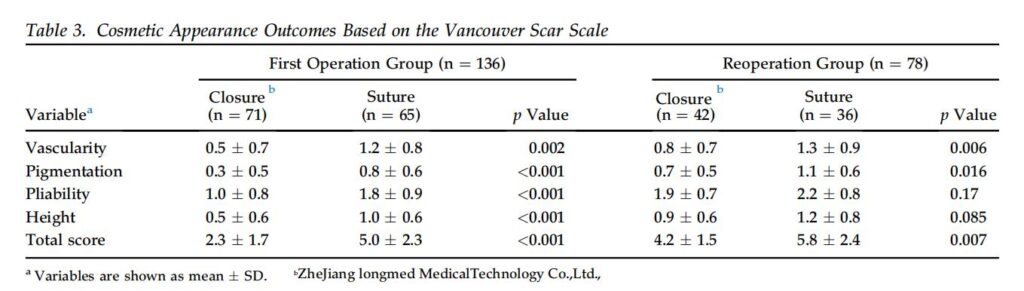
外観
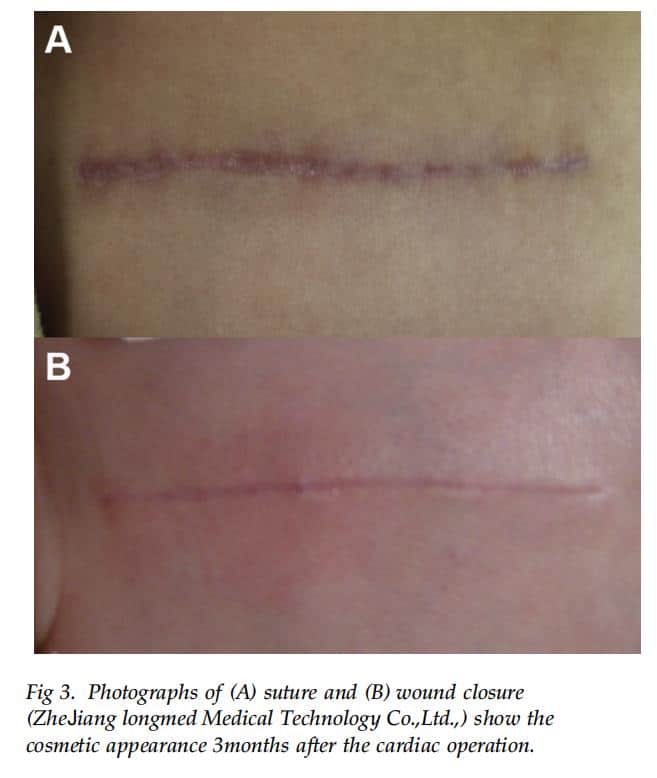
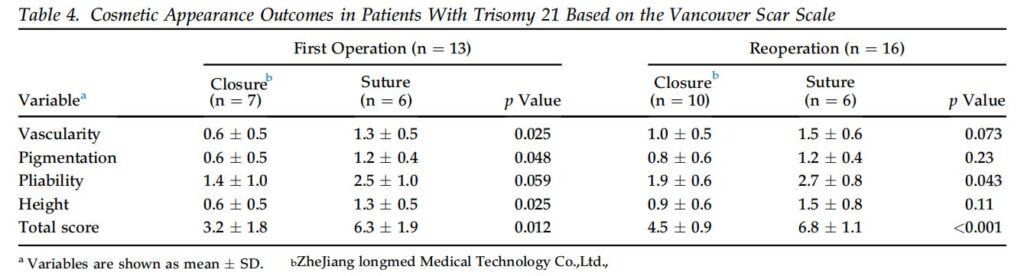
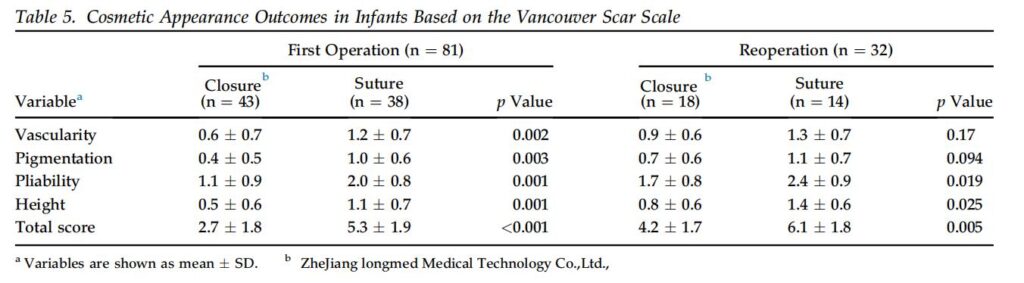
美容的外観は、手術後 3 か月後に VSS によって評価されました (図 3)。 FO グループでは、すべての VSS 変数において、閉鎖グループの VSS は縫合グループよりも有意に低かった (表 3)。 RO グループでは、血管分布、色素沈着、および合計 VSS スコアは、縫合グループよりも閉鎖グループの方が有意に低かった。さらに、21トリソミー患者の合計VSSスコアは、縫合群と比較して閉鎖群で有意に低かった(表4)。さらに、乳児の合計VSSスコアは、縫合群より閉鎖群で有意に低かった(表4)。 5)。同様に、新生児では、閉鎖グループの合計 VSS スコアは縫合グループの合計 VSS スコアよりも有意に低かった (3.0 ± 2.0 対 5.2 ± 2.3、p < 0.017)。 2 人の外科医の間で、創傷閉鎖 (p = 0.96) および縫合 (p = 0.79) の VSS スコアに有意差はありませんでした。
創傷閉鎖装置の皮膚閉鎖時間
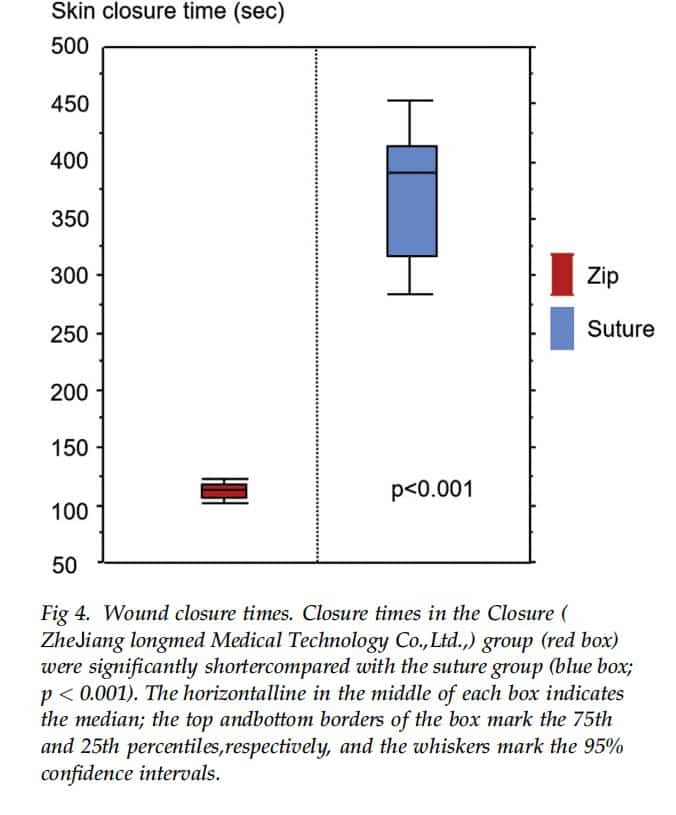
Closure 群と縫合群の総手術時間の差 (340.3 127.1 分 vs 328.2 120.7 分) は有意ではなかった (p = 0.70)。しかしながら、Closure 群の皮膚閉鎖時間は縫合群のそれより有意に短かった。縫合糸グループ (113.0 9.1 秒 vs 375.9 60.2 秒、p <0.001; 図 4)。皮膚閉鎖時間の中央値は、閉鎖グループでは 113 秒 (範囲、98 ~ 135 秒)、縫合グループでは 389 秒 (範囲、256 ~ 470 秒) でした。
合併症と身体所見
合併症率は閉鎖群(n = 113)と縫合群(n = 101)の間で比較されました。手術創感染は閉鎖群では 1 名、縫合群では 2 名で発生しました。外科的感染率は閉鎖群と縫合群の間で有意な差はありませんでした(0.9% vs 2.0%、p = 0.50)。3人の患者は手術部位感染症を患っていましたが、重度ではなく、抗生物質と食塩水での洗浄で改善しました。手術創の裂開は閉鎖群の患者 2 名、縫合群の患者 3 名で発生しました。 2 つのグループ間で手術創の裂開に有意差はありませんでした (1.8% 対 3.0%、p = 0.56)。創傷裂開が発生したすべての患者は新生児または 21 トリソミーでした。閉鎖デバイスに特有の合併症としては、皮膚の変色 (0.9%)、表皮剥離 (0.9%)、およびデバイスの剥離 (1.8%) が含まれます。粘着テープの吹き出物により変色が生じたが、ステロイド軟膏の塗布により改善した。表皮剥離も軟膏で治療しました。装置が剥がれた患者には新しい装置を貼り付けた。
ただし、デバイスに対するアレルギーや損傷などの重篤な合併症は発生しませんでした。乳児を含む小児患者はかゆみや痛みを訴えることができなかったため、かゆみや痛みを評価することはできませんでした。
しかし、創傷閉鎖装置または縫合糸の除去中に、縫合群と比較して閉鎖群では泣いたり訴えたりする患者の数が有意に少なかった(7.1% vs 52.5%、p < 0.001)。
コメント
この研究は、心臓手術を受けた小児患者を対象とした創傷閉鎖装置の最初のランダム化対照試験です。創傷閉鎖装置に関連した最近の症例報告がいくつか報告されていますが、胸骨正中切開による心臓手術については報告されていません[7、8]。また、小児患者における利点や合併症のリスクも不明のままです。私たちの研究では、胸骨正中切開による心臓手術を受けた小児患者を評価しました。私たちの結果は、縫合糸グループと比較して閉鎖グループの方が有意に良い結果を示しました。電気メスの使用、感染、アプローチ、縫合糸の素材など、多くの要因が手術創の外観に影響を与えることを考慮すると、[13-15] 、一貫した外科的切開アプローチと縫合材料を使用し、すべての患者で胸骨正中切開を行うために電気メスが使用されました。私たちの結果は、最初の手術か再手術かに関係なく、創傷閉鎖デバイスには美容上の利点があることが実証されました。小児心臓外科では、多くの患者が 21 トリソミーを患っています [16]。さらに、心臓欠陥のある小児患者の場合、心臓手術は乳児期に行われることが多い[17、18]。
この試験の結果に基づいて、この創傷閉鎖デバイスは幅広い患者にうまく使用できると考えています。
閉鎖時間の点では、創傷閉鎖デバイスを使用して閉鎖した手術創傷は、縫合糸を使用した創傷閉鎖と比較して明らかに優れた性能を示しました。同様に、2-オクチルシアノアクリレート接着剤の使用も、外科的創傷閉鎖時間を短縮できます [4、19]。しかし、オクチルシアノアクリレートが胸骨正中切開術に使用されたという報告はなく、創傷閉鎖装置との安全性および閉鎖時間の比較が困難となっています。この研究では、
閉鎖グループにおける皮膚閉鎖時間の時間的分散は非常に小さかった。これは、このデバイスの使用が創傷の長さや異なる外科医による影響を受けなかったことを意味する。したがって、傷が長ければ長いほど、相対的に大きな利益が期待できます。
Closure グループと縫合糸グループの間の手術創感染率の差は有意ではありませんでしたが、Closure グループでは創傷感染の発生が少なかったです。小児心臓手術後の手術部位感染の発生率は、2.3%から8%の範囲であると報告されている[20-23]。この研究では、Closure グループにおける術後創傷感染の発生率は 0.9% であり、Closure グループの表皮に残存物がなかったことを考慮すると、感染率は非常に低い値です。肥厚性瘢痕が報告されている [24-26]。ただし、創傷閉鎖デバイスには、創傷閉鎖時間を短縮するという追加の利点もあります。
手術創の感染症や手術跡の予防に加えて。
創感染率と同様に、Z 群の手術創裂開発生率も縫合糸群と同等以上でした。しかしながら、創傷閉鎖デバイスは、創傷裂開に対してより大きな柔軟性を有し、より非侵襲的である。研究デザインに従って、手術の 7 日後に縫合糸またはデバイスを取り外しました。ただし、新生児および 21 トリソミー患者では創部裂開が観察されたのみであるため、創傷状態に応じてデバイスの除去を行う必要があると考えられます。この装置に特有の合併症としては、皮膚の変色、表皮剥離、装置の剥離などが挙げられますが、いずれも高率に発生したり重篤なものではありませんでした。その結果、創傷閉鎖デバイスは安全に使用できると結論付けました。
創傷閉鎖装置の優れた特徴は、その長さと張力を調整できることです。デバイスの長さは、デバイスを適切な位置で切断することで簡単に調整できます。適応ストラップロックシステムにより、デバイスの張力を無制限に調整できます。たとえば、手術後の浮腫や創傷治癒の程度に応じて、デバイスの張力を複数回調整することができます。また、ジッパーを外すことで傷の治り具合を確認することができます。したがって、このデバイスは、縫合糸を必要とせずに、ジッパーを再度揺動させることによって裂開に対応できます。
この研究の結果から、創傷閉鎖デバイスを使用する最大の利点は、優れた外観と閉鎖時間の短縮であると考えられます。また、このデバイスの安全性は皮下縫合糸と同様に良好でした。しかし、創傷閉鎖装置の際立った特徴は、取り外す際の痛みが少ないことであり、特に小児患者にとって有益でした。実際、Closureグループでは、縫合グループに比べてデバイスや抜糸の際に痛みを感じたり、泣いたりする患者が大幅に少なかった。逆に、創傷閉鎖デバイスのコストパフォーマンスは縫合グループに及ばない。創傷閉鎖デバイスの価格は $85 で、皮下縫合糸の約 3 倍高価ですが、その美容効果と閉鎖時間の有効性を考慮すると、このデバイスを使用する価値は十分にあると考えます。
現在の研究にはいくつかの限界があります。まず、この研究は単一の施設で実施されました。したがって、私たちの結果の一般化には限界があります。しかし、これは胸骨正中切開を受けた小児患者における創傷閉鎖デバイスの使用を報告した最初の前向きランダム化試験であるため、これらのデータは重要です。
第二に、ダウン症患者の数は比較的少ないため、ダウン症患者におけるデバイスの効率を評価するには統計的検出力が不十分です。
第三に、この研究では、21トリソミーを除く染色体異常のある患者および胸骨閉鎖が遅れた患者は除外された。したがって、それらの集団における結果を調査することはできませんでした。装置と技術に関しては、非吸収性ポリプロピレン縫合糸を使用して抜糸を伴う連続皮下縫合術は珍しい方法である可能性があります。最後に、この研究は小児患者を対象としたランダム化試験であり、成人患者における有効性は検討していません。したがって、成人集団におけるデバイスの使用を検証するには、成人患者を対象とした前向きランダム化臨床試験が必要です。
結論として、これは胸骨正中切開による心臓手術を受けた小児患者を対象としたジップステッチ Longmed 創傷閉鎖デバイスの結果を評価する最初のランダム化試験です。私たちの研究では、この装置が美容上の外観を改善し、皮膚の閉鎖時間を短縮する点で優れた性能を備えていることがわかりました。これは簡単かつ安全に使用できる非侵襲的な装置であり、痛みが少ないため小児患者に適していると考えられます。
参考文献
- Jina H、Simcock J. 胸骨正中切開傷跡の評価。 NZ Med J 2011;124:57–62。
- Cotogni P、Barbero C、Rinaldi M. 心臓手術後の胸骨深部創感染:証拠と論争。 World J Care Med 2015;4:265–73。
- Lemaignen A、Birgand G、Ghodhbane W 他心臓手術後の胸骨創傷感染:臨床症状に応じた発生率と危険因子。 Clin Microbiol Infect 2015;21:674.e11–18。
- Krishnamoorthy B、Najam O、Kharn UA、Waterworth P、Fildes JE、Yonan N。伏在静脈採取後の従来の皮下皮膚閉鎖術とダーマボンド皮膚接着剤を比較したランダム化前向き研究。アン・ソラック・サーグ、2009;88:1445–50。
- Chambers A、Scarci M. シアノアクリレート接着剤による皮膚閉鎖は胸骨創傷感染の予防に効果的です。Interact CardioVasc Thorac Surg 2010;10:793–6。
- ラヴァッツォ C、グケグケス ID、ヴロウマヌー EK、ママイス I、ペパス G、ファラガス ME。外科的創傷の管理における縫合糸とステープル: ランダム化対照試験のメタ分析。 Am Surg2011;77:1206–21。
- Gorsulowsky DC、Talmor G。皮膚閉鎖の最終層としての新しい非侵襲性創傷閉鎖デバイス。 Dermatol Surg 2015;41:987–9。
- マリアED。新しい皮膚閉鎖システムは、心臓血管埋め込み型電子機器手術後の創傷治癒を促進します。 World J Clin Cases 2015;3:675–7。
- ペ・SH、ペ・YC。傷跡の状態と治療方法に基づいた、さまざまな傷跡評価スケールの使用頻度の分析。 Arch Plast Surg 2014;41:111–5。
- Truong PT、Abnousi F、Yong CM、他バンクーバー瘢痕スケール、短縮形式のマギル疼痛アンケート、および患者の視点を統合した、乳がんの手術痕の標準化された評価。 Plast Reconstr Surg 2005;116:1291–9。
- Lee SH、Zheng Z、Roh MR.二酸化フラクショナルレーザーを使用した手術瘢痕の術後早期治療: 分割瘢痕、評価者盲検研究。 Dermatol Surg 2013;39:1190–6。
- Femonti R、Bond J、Erdmann D、Levinson H. 傷跡および傷跡測定装置のレビュー。エプラスティ 2010;10:e43。
- 歌手AJ、クインJV、ソーデHCジュニア、ホランダーJE。裂傷および外科的切開修復後の予後不良の決定要因。 Plast Reconstr Surg 2002;110:429–37。
- Niessen FB、Spauwen PH、Kon M. 肥厚性瘢痕形成における縫合糸材料の役割: モノクリル対ビクリルラピド。アン・プラスト・サーグ、1997;39:254–60。
- クロスランド DS、ジャクソン SP、ライアル R 他胸骨切開術と胸郭切開術の傷跡に対する患者の態度。胸部心臓血管外科 2005;53:93–5。
- フリーマンSB、タフトLE、ドゥーリーKJ 他ダウン症候群の先天性心疾患に関する集団ベースの研究。 Am J Med Genet 1998;80:213–7。
- Moller J. 心臓奇形の有病率と発生率。出典: Moller JH (編)。小児心臓病学における展望:先天性心疾患の手術:小児心臓ケアコンソーシアム、1984-1995年。ニューヨーク州アーモンク:フューチュラ。 1998: 619–26。
- ディキンソンDF、アーノルドR、ウィルキンソンJL。 1960年から1969年にかけてリバプールで生まれた16万480人の先天性心疾患。外科的治療への影響。 Br Heart J 1981;46:55–62。
- クイン J、ウェルズ G、サトクリフ T、他。裂傷の管理においてオクチルシアノアクリレート組織接着剤と縫合糸を比較するランダム化試験。 JAMA 1997;277:1527–30。
- バーカー GM、オブライエン SM、ウェルケ KF 他小児心臓手術後の大感染症: リスク推定モデル。アン・ソラック・サーグ、2010;89:843–50。
- ポロック EM、フォード・ジョーンズ EL、レベイカ I 他小児心臓血管外科患者における初期の院内感染。クリティカルケアメッド 1990;18:378–84。
- Levy I、Ovadia B、Erez E. 乳児および小児における心臓手術後の院内感染: 発生率と危険因子。 J Hosp Infect 2003;53:111–6。
- オールプレス AL、ローゼンタール GL、グッドリッチ KM、ルピネッティ FM、ザー DM。小児心臓血管手術後の手術部位感染の危険因子。 Pediatr Infect Dis J 2004;23:231–4。
- Chan KY、Lau CL、Adeeb SM、Somasundaram S、NasirZahari M。胸骨正中切開創傷における肥厚性瘢痕の発生を予防するシリコーンゲルのランダム化プラセボ対照二重盲検前向き臨床試験。 Plast Reconstr Surg 2005;116:1013–20。
- 桜庭 M、高橋 N、赤星 T、宮坂 Y、鈴木 K. 胸骨正中切開後のケロイド瘢痕患者に対するシリコーン ゲル シートの経験。 Gen Thorac Cardiovasc Surg 2010;58:467–70。
- Pai VB、Cummings I. 胸骨切開後のケロイド瘢痕に対する良い治療法はありますか? Interact Cardiovasc Thorac Surg 2011;13:415–8。
